רטיניטיס פיגמנטוזה
 | |
| ראייה תקינה (למעלה) לעומת ראיית אדם עם רטיניטיס פיגמנטוזה (ראיית מנהרה) בשלב מתקדם (למטה) | |
| שמות נוספים | RP |
|---|---|
| תחום |
רפואת עיניים |
| שכיחות | 1/4000 (0.025%) |
| גורם | גנטי |
| תסמינים | עיוורון לילה, ראיית מנהרה |
| אבחון | לפי תסמינים קליניים, שדות ראייה, ממצאים בקרקעית העין, אלקטרורטינוגרפיה, טומוגרפיה אופטית קוהרנטית. |
| טיפול |
לוקסטורנה |
| קישורים ומאגרי מידע | |
| MeSH | D012174 |
| סיווגים | |
| ICD-10 | Code H35.52 |
רטיניטיס פיגמנטוזה (באנגלית: Retinitis pigmentosa) היא מחלת עיניים ניוונית של הרשתית, הנפוצה ביותר מבין מחלות ניוון רשתית בעלות רקע תורשתי. המחלה גורמת באופן פרוגרסיבי לעיוורון לילה ולהיצרות שדות הראייה, לעיתים עד כדי עיוורון מוחלט.
היסטוריה
[עריכת קוד מקור | עריכה]בשנת 1744 תיעד רופא העיניים הגרמני רודיגר אופלגון (Rüdiger F. Ovelgün) מקרה של עיוורון לילה בקרב בני משפחה אחת. מקרה זה נחשב לתיעוד הראשון של המחלה.[1]
בתחילת המאה ה-19 דיווחו רופאים נוספים (Schon, 1828; Von Ammon, 1838) על חולים עם ראייה לקויה שהתגלו אצלם פיגמנטים מרובים בקרקעית העין (פונדוס).[1]
בשנת 1853 תיאר הרופא ההולנדי אדריאן ואן טריכט (Adrien van Trigt) את צורות הפיגמנטים ברשתית העין (מופע ייחודי למחלה), אותן הצליח לראות לראשונה באמצעות אופטלמוסקופ.[1][2]
אטימולוגיה
[עריכת קוד מקור | עריכה]את המונח "רטיניטיס פיגמנטוזה" טבע רופא העיניים ההולנדי פרנסיסקוס דונדרס בשנת 1857. הוא כינה אותה רטיניטיס (דלקת רשתית) בשל תפיסה שגויה שמדובר בדלקת. את הביטוי פיגמנטוזה טבע דונדרס על שם הממצא הפיגמנטרי בקרקעית העין שגילה אצל הלוקים במחלה ואשר נפוץ ברוב המקרים.[3]
אנטומיה
[עריכת קוד מקור | עריכה]
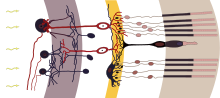
רטיניטיס פיגמנטוזה היא מחלה הגורמת לרשתית העין לצאת באופן הדרגתי מכלל פעולה תקינה. הרשתית היא שכבת תאים בחלק האחורי של גלגל העין המכילה תאים קולטי אור: תאי קנים, תאי מדוכים ותאי גנגליון קולטי אור, הממירים אור לאותות עצביים המפוענחים על ידי המוח ומייצרים את התפיסה החזותית.[4]
הרשתית מורכבת מעשר שכבות:
- ממברנה מגבילה פנימית - השכבה הפנימית ביותר של הרשתית היוצרת גבול עם תא הזגוגית של העין. הגבול ההיקפי של שכבה זו מורכב מתאי מולר(אנ'), ששומרים על הומאוסטאזיס ברשתית על ידי שמירה על למינציה ברשתית ועל ידי תמיכה בתאים נוספים. הממברנה המגבילה הפנימית משמשת כשכבה למינלית בסיסית(אנ') עבור תאי שכבת סיבי עצב הרשתית.
- שכבת תאי הגנגליון - שכבת גופי תאי הגנגליון המשגרים את האקסונים שלהם, ובסופו של תהליך יוצרים את עצב הראייה.
- שכבת סיב עצב - השכבה המורכבת מאקסונים של תאי הגנגליון (אנ') ברשתית המעורבבים עם אסטרוציטים ותאי מולר.
- שכבת פרספקס פנימית - שכבה זו היא המקום שבו האקסונים של התאים הדו-קוטביים מסתנפים אל תאי הגנגליון. הדנדריטים של תאים אקריניים גם הם סינפסים באזור זה, ופועלים לוויסות ההולכה החשמלית בין התאים הדו-קוטביים ותאי הגנגליון.
- שכבה גרעינית פנימית - שכבה המורכבת מתאים דו-קוטביים, תאים אופקיים ותאים אקריניים. תאים דו-קוטביים מתפקדים כערוצים המשדרים ומקודדים תשומות סינפטיות שונות מתאי קולטני האור אל תאי הגנגליון, אל תאי הקנים ואל תאי המדוכים.
- השכבה הפלקסיפורמית החיצונית - האזור שבו ההקרנות מתאי הפוטו-קולטס מסתנפות אל הדנדריטים של התאים השוכנים בשכבה הגרעינית הפנימית.
- שכבה גרעינית חיצונית - השכבה המכילה את גופי התא של תאי הקנים ותאי המדוכים כאחד.
- ממברנה מגבילה חיצונית - התחום שבין תאי פוטורצפטורים לתאי מולר; התחום מפריד בין גופי התא של תאי הקנים והמדוכים מהמקטעים הפנימיים והמקטעים החיצוניים שלהם.
- שכבת תאים קולטי אור - השכבה מורכבת מהמקטעים הפנימיים ומהמקטעים החיצוניים של תאי הקנים והמדוכים. מקטעי הפוטו-קולטן החיצוניים מורכבים מדיסקים הקשורים לממברנה ומכילים את הפיגמנטים הרגישים לאור, כגון רודופסין, הנחוצים להתמרה חזותית (Visual phototransduction). המקטעים הפנימיים מכילים את שפע המיטוכונדריה הדרוש כדי לעמוד בדרישות המטבוליות הגבוהות של תאי הפוטו-קולטן.
- אפיתל פיגמנט הרשתית - שכבת הרשתית החיצונית ביותר המשתרעת על רוחב של תא בודד הממוקמת בין הרשתית העצבית לממברנה של ברוך (אנ'), בסמוך לשכבת הכורואיד. אפיתל הפיגמנט ברשתית (RPE) תורם למחסום רשתית בשילוב עם האנדותל של כלי הרשתית, ויש לו תפקידים רבים, כולל הובלת יונים ומים והפרשת גורמי גדילה וציטוקינים. תאי RPE מתערבבים עם המקטעים החיצוניים של תאי הקנים והמדוכים. קרבה זו מאפשרת התמרה חזותית, תאי RPE הם חיוניים בתמיכה ובתחזוקה של תאי קולטני אור ושל האנדותל הנימי הבסיסי.[5][6]
פיזיולוגיה
[עריכת קוד מקור | עריכה]הרשתית בנויה מקולטני אור הכוללים תאי קנים (Rod cells) הפועלים באור חלש ועמום (ראייה סקוטופית) ומשמשים לראיית לילה. תאים אלו נפגעים ראשונים ברטיניטיס פיגמנטוזה וגורמים באופן הדרגתי לעיוורון לילה ולהיצרות שדות הראייה. תאי המדוכים (Cone cells) אחראים על חדות הראייה וראיית צבעים (ראייה פוטופית), ומשמשים בראיית יום. התאים ממוקמים באופן יחסי רחוק יותר מהאישון שדרכו חודר האור לעין. המדוכים ממוקמים במרכז הרשתית, בפוביאה. ישנם כ-6 מיליון תאי מדוכים ויותר מ-100 מיליון תאי קנים בתוך הרשתית.
קיימים שלושה סוגים של תאי מדוכים: טריטנים (tritans), דוטרנים (deutrans) ופרוטאנים (protans), על שם זיהוי אורכי גל קצרים, בינוניים וארוכים, בהתאמה. כל תא אור מסוג מדוך הוא בעל יכולת זיהוי אורכי גל כחול, ירוק ואדום, ובכך מאפשר ראיית צבעים.[7]
מאפייני התמונה הקלינית
[עריכת קוד מקור | עריכה]
בשלב הראשון מתבטאת המחלה בירידה בראיית לילה עד כדי עיוורון לילה, ובירידה הדרגתית בראייה ההיקפית עד כדי ראיית מנהרה. למאפיינים אלה מתלווה לעיתים גם קוצר ראייה.
התקדמות המחלה מתרחשת בשתי העיניים בדפוס דומה אך לא זהה.[8] הראשונים להיפגע הם תאי הקנים, האחראים על ראיית לילה וממוקמים בעיקר בהיקף הרשתית. הירידה ביכולת קולטני האור לקלוט פוטונים מתקדמת במהירות יחסית לשדה ההיקפי הרחוק, ובסופו של דבר מתרחבת אל שדה הראייה המרכזי (מקולה) ככל שהם מתנוונים. חדות הראייה וראיית הצבעים עלולות להיפגע גם הן עקב אובדן נלווה של תאי המדוכים.
מעבר להשפעות הישירות של ניוון הקולטנים, מאופיינת רטיניטיס פיגמנטוזה במגוון של תסמינים עקיפים. תופעות כמו פוטופוביה, שבה האור נתפס כסנוור עז ופוטופסיה, הופעה של אורות מהבהבים, מתערבלים או מנצנצים המתרחשים באופן ספונטני בתוך שדה הראייה, מאפיינת לעיתים קרובות את שלביה האחרונים של המחלה.[9] ראיית סריג (latticework vision) מתרחשת לעיתים ברטיניטיס פיגמנטוזה כולל בתסמונות גנטיות מורכבות דוגמת תסמונת בארדט-בידל.[10]
לעיתים יש למחלה השפעות פסיכולוגיות שליליות על הלוקים בה. במחקר שפורסם בשנת 2015 בכתב העת המדעי European Journal of Ophthalmology נבדקו 34 חולים במחלה מול קבוצת ביקורת של אנשים ללא לקות ראייה. התגלה כי החולים במחלה מראים תסמינים של דיכאון קל עד בינוני, בהשוואה לקבוצת הביקורת של נסיינים בריאים ללא לקות ראייה. ישנו מתאם בין תסמינים אלו לבין חומרת המחלה וגיל הנבדק, דבר המצביע על כך שהחמרה במצב הראייה וגיל מבוגר יותר בחולים בה עלולים להוות גורם לדיכאון.[11]
אטיולוגיה
[עריכת קוד מקור | עריכה]
המחלה נגרמת עקב אפופטוזה,[12] סוג של מוות תאי מתוכנת של תאי הקולטנים (פוטורצפטורים) ברשתית העין. אפופטוזה, לפי המחקר, היא המנגנון הביולוגי השולט במחלות ניווניות, לרבות מחלות ניוון הרשתית. התחלת אפופטוזה תלויה בהפעלה של חלבוני קספאז. הפעלה פנימית של אפופטוזה באמצעות זיהוי נזק לתאים מובילה לביטוי מוגבר של חלבונים פרו-אפופטוטיים, כגון מווסת אפופטוזיס BAX, וכתוצאה מכך לשחרור חלבונים מיטוכונדריאליים, כולל ציטוכרום. שחרור זה גורם לתהליך מורכב המסתיים בפיצול DNA וחלבונים, עיבוי כרומטין ויצירת גופים אפופטוטיים. אפופטוזה עלולה להתרחש גם באופן חיצוני בעקבות אינטראקציה בין ליגנדים המיוצרים על ידי תאי מערכת החיסון לבין קולטני מוות (כגון Tumor Necrosis Factor (TNF)(אנ') או Fas(אנ')) על פני השטח של תאים פגומים. קולטנים הקשורים ל-Fas ligand(אנ') מפעילים את החלבון קספאז, וזה מוביל בסופו של דבר להפעלה של קספאזי תליין (executioner caspases) ויצירת גופים אפופטוטיים המובילים למוות הדרגתי של תאי האור.[13]
גנטיקה
[עריכת קוד מקור | עריכה]המחלה היא גנטית (תורשתית), ונגרמת כתוצאה ממוטציה גנטית. ידועות מעל אלף מוטציות שונות בלמעלה מ-60 גנים שעלולות לגרום למחלה. מחקר גנטי המתבצע במעבדות שונות בארץ הוביל לאיתור חלק מהגנים הנפוצים באוכלוסיית ישראל.[14]
ישנם גנים רבים המקודדים לחלבונים הדרושים לתפקוד קולטני האור. כאשר גנים אלה עוברים מוטציה, הם עלולים לגרום לפנוטיפ המתבטא באחד או יותר ממאפייני המחלה. דפוסי התורשה של רוב הלוקים במחלה תלויים במוטציות הספציפיות של הגן הקיימות בדור ההורים וזוהו כמתנהגים לפי כל אחת מהדרכים הקלאסיות הידועות: אוטוזומלים דומיננטיים, אוטוזומלים רצסיביים, בתאחיזה לכרומוזום X וצורת הורשה מיטוכונדרית.[15]
צורות הורשה אוטוזומליות דומיננטיות ורצסיביות של רטיניטיס פיגמנטוזה משפיעות באופן שווה על גברים ונשים. עם זאת, הצורה הפחות שכיחה של המחלה קשורה לתאחיזה לכרומוזום X,[16] ומשפיעה על גברים בעלי המוטציה המסוימת הזו, בעוד שנשים הן נשאיות בלבד. צורת הורשה זו מובילה לרוב למופע קשה של המחלה, עד כדי עיוורון מוחלט בשלבים מאוחרים יותר. במקרים נדירים, צורה דומיננטית של מוטציית הגן המקושרת לכרומוזום X משפיעה באופן שווה על זכרים ונקבות.[17]
| גנים נפוצים אצל הלוקים ברטיניטיס פיגמנטוזה[18] | ||
|---|---|---|
| OMIM | גן | סוג של רטיניטיס פיגמנטוזה ו/או צורת הורשה |
| 400004 | RPY | רטיניטיס פיגמנטוזה בתאחיזה לכרומוזום Y |
| 180100 | RP1 | רטיניטיס פיגמנטוזה 1 |
| 312600 | RP2 | רטיניטיס פיגמנטוזה 2 |
| 300029 | RPGR | רטיניטיס פיגמנטוזה 3 |
| 608133 | PRPH2 | רטיניטיס פיגמנטוזה 7 |
| 180104 | RP9 | רטיניטיס פיגמנטוזה 9 |
| 180105 | IMPDH1 | רטיניטיס פיגמנטוזה 10 |
| 600138 | PRPF31 | רטיניטיס פיגמנטוזה 11 צורת הורשה אוטוסומלית דומיננטית |
| 600105 | CRB1 | רטיניטיס פיגמנטוזה 12 צורת הורשה אוטוסומלית רצסיבית |
| 600059 | PRPF8 | רטיניטיס פיגמנטוזה 13 |
| 600132 | TULP1 | רטיניטיס פיגמנטוזה 14 |
| 600852 | CA4 | רטיניטיס פיגמנטוזה 17 |
| 601414 | HPRPF3 | רטיניטיס פיגמנטוזה 18 |
| 601718 | ABCA4 | רטיניטיס פיגמנטוזה 19 |
| 602772 | EYS | רטיניטיס פיגמנטוזה 25 |
| 608380 | CERKL | רטיניטיס פיגמנטוזה 26 |
| 606068 | FAM161A[19] | רטיניטיס פיגמנטוזה 28 צורת הורשה אוטוסומלית רצסיבית, הגן נפוץ |
| 607921 | FSCN2 | רטיניטיס פיגמנטוזה 30 |
| 609923 | TOPORS | רטיניטיס פיגמנטוזה 31 |
| 610359 | SNRNP200 | רטיניטיס פיגמנטוזה 33 |
| 610282 | SEMA4A | רטיניטיס פיגמנטוזה 35 |
| 610599 | PRCD | רטיניטיס פיגמנטוזה 36 |
| 611131 | NR2E3 | רטיניטיס פיגמנטוזה 37 |
| 268000 | MERTK | רטיניטיס פיגמנטוזה 38 |
| 268000 | USH2A (אנ') | רטיניטיס פיגמנטוזה 39, בנוסף ללקות שמיעה כחלק מתסמונת אשר |
| 612095 | PROM1 | רטיניטיס פיגמנטוזה 41 |
| 612943 | KLHL7 | רטיניטיס פיגמנטוזה 42 |
| 268000 | CNGB1 | רטיניטיס פיגמנטוזה 45 |
| 613194 | BEST1 | רטיניטיס פיגמנטוזה 50 |
| 613464 | TTC8 | רטיניטיס פיגמנטוזה 51 |
| 613428 | C2orf71 | רטיניטיס פיגמנטוזה 54 |
| 613575 | ARL6 | רטיניטיס פיגמנטוזה 55 |
| 613617 | ZNF513 | רטיניטיס פיגמנטוזה 58 |
| 613861 | DHDDS | רטיניטיס פיגמנטוזה 59 |
| 613194 | BEST1 | רטיניטיס פיגמנטוזה קונצנטרי |
| 608133 | PRPH2 | |
| 613341 | LRAT | רטיניטיס פיגמנטוזה אצל ילדים |
| 268000 | SPATA7 | רטיניטיס פיגמנטוזה אצל ילדים צורת הורשה אוטוסומלית רצסיבית |
| 268000 | CRX | רטיניטיס פיגמנטוזה, צורת הורשה דומיננטית מאוחרת |
| 300455 | RPGR | רטיניטיס פיגמנטוזה, בתאחיזה לכרומוזום X, עם או בלי חירשות |
אבחנה
[עריכת קוד מקור | עריכה]את המחלה מאבחנים באמצעות מספר בדיקות:
- מיפוי גנטי - בדיקה המשמשת לזיהוי שינויים ברצף ה-DNA או במבנה הכרומוזומים המובילה לאיתור גנים המחוללים את המחלה.
- בדיקת הרחבת אישונים - בדיקת קרקעית עין מורחבת (DFE) היא הליך אבחוני המשתמש בהרחבת האישונים על מנת לקבל מבט מדויק ופרטני יותר על קרקעית העין. הליך זה משמש לאיתור פיגמנטים בקרקעית. ממצאים הקשורים למחלה מאופיינים פעמים רבות בהתפתחות פיגמנטים בקרקעית העין.[22][23]
- אלקטרורטינוגרפיה (ERG) - בדיקה אלקטרופיזיולוגית בתחום האופטומטריה והאופטלמולוגיה, שמשמשת לאיתור ומיקום ליקויים בתפקוד רשתית העין.[24]
- טומוגרפיה אופטית קוהרנטית (OCT) - שיטת הדמיה (דימות) אופטית קוהרנטית, המבוססת על אינטרפרומטריה ופיזור של גלי אור בתחום האינפרא אדום. בעזרתה ניתן להפיק תמונות תלת־ממדיות באיכות גבוהה של רקמות ביולוגיות, ובהן של הרשתית.
- בדיקת שדות ראייה - בדיקה מתחום האופטומטריה הבוחנת את תקינות תחום הראייה הפריפריאלית (היקפית).[25]
לעיתים האבחון כולל צילומי עין מסוג בדיקת אוטופלואורסצנציה של קרקעית העין.[26][27]
מופע לא פיגמנטרי
[עריכת קוד מקור | עריכה]בחלק קטן מהמקרים מופיעה המחלה בצורה לא פיגמנטרית. הצורה הלא-פיגמנטרית של רטיניטיס פיגמנטוזה מהווה לעיתים שלב מוקדם של המחלה ולא מופע חריג. רוב המטופלים שאובחנו ללא השינויים הפיגמנטריים האופייניים הראו פגיעה קלה יותר בתפקוד הרשתית.
במחקר נבדקו 68 חולים עם רטיניטיס פיגמנטוזה על מנת לקבוע את תדירות המופע. התגלתה שכיחות של 22% מכלל הנבדקים. בהיעדר ממצאים פיגמנטריים, ניתן לאבחן את המחלה לפי היסטוריה משפחתית של עיוורון לילה, אובדן שדה ראייה היקפי ותגובה אלקטרורטינוגרפית לקויה או חסרה.[28]
מופע חלקי (Sector RP)
[עריכת קוד מקור | עריכה]
מופע סקטוריאלי (חלקי) של המחלה (נקרא גם sine pigmento) הוא צורה נדירה המופיעה בהשפעתן של מספר מוטציות גנטיות שבה רק בחלק מרשתית אחת או שתי הרשתיות ישנם סימנים פתולוגיים קליניים. המחקר הראה פגיעה בחלקים התחתונים של הרשתית, לעיתים ברבע אחד בלבד. צורה זו של המחלה היא לרוב בעלת מאפיינים קלים יותר, וקצב התפתחותה איטי באופן יחסי.[29][30]

אבחנה מבדלת
[עריכת קוד מקור | עריכה]קיימים מצבים רפואיים, מחלות ותסמונות הגורמים לממצאים אופטלמוסקופים הדומים או זהים לרטיניטיס פיגמנטוזה, הכוללים דלקת עיניים הקשורה לזיהום בגיל מוקדם, אדמת, עגבת, חצבת, טוקסופלזמוזיס, היפרדות רשתית, אובאיטיס, רטינופתיה אוטואימונית פארא-נאופלסטית, רטינופתיה פיגמנטרית, חסימת עורק רשתית מרכזית (CRAO), רעילות תרופתית הנגרמת על ידי תרופות כגון: כלורוקווין, כינין ופנותיאזין, וכן טראומה בעיניים כגון צלקות מקרני לייזר. מצבים אלו יכולים להתרחש בעין אחת או בשתיהן באופן סטטי או בצורה פרוגרסיבית.[31][32]
רטיניטיס פיגמנטוזה (RP) מופיעה בכמה תצורות: (1) כמחלה לא סינדרומטית (ללא כל ממצא קליני נוסף), (2) כחלק מתסמונת עם הפרעות נוירו-חושיות אחרות, הפרעות התפתחותיות או ממצאים קליניים מורכבים, (3) כפגיעה משנית למחלה מרכזית ומורכבת אחרת.[33]
- RP בשילוב עם חירשות (מולדת או פרוגרסיבית) נקראת תסמונת אשר.[34]
- תסמונת אלפורט מופיעה לעיתים בשילוב עם אחד המופעים הקלים של רטיניטיס פיגמנטוזה (sine pigmento).[35][36]
- RP בשילוב עם מוגבלות שכלית התפתחותית, נוירופתיה פריפרית, אטקסיה, סטיאטוריה כחלק מתסמונת קרנס-סייר.[37]
- RP מופיעה במספר הפרעות גנטיות נדירות אחרות (כולל ניוון שרירים ומחלה גרנולומטית כרונית) כחלק מתסמונת מקלאוד.[38]
- RP מופיעה במספר תסמונות: נוירוסיפיליס (אנ'), טוקסופלזמוזיס ומחלת רפסם.[39]
- RP הקשורה להיפוגונדיזם ועיכוב התפתחותי עם דפוס תורשה אוטוזומלית רצסיבית, תועדה בתסמונת בארדט-בידל.[40]
טיפול
[עריכת קוד מקור | עריכה]בשנת 2017 אושרה על-ידי ה-FDA התרופה לוקסטורנה המהווה טיפול גנטי חלקי למחלה, לבעלי מוטציות שונות בגן RPE65 הנמצאים בשלב הראשוני של המחלה.[41][42] התרופה מספקת עותק תקין (לא מוטציוני) של הגן RPE65 כדי שיתפקד במקום הגן RPE65 שעבר מוטציה. הגן RPE65 התקין יוצר את החלבון בגן RPE65, ובכך משחזר את יכולת הראייה.[43]
ישנם כמה אפיקי מחקר שמכוונים להביא לטיפול חלקי או מלא בגנים נוספים שגורמים למחלה, אך נכון לתחילת 2024 טרם הבשיל המחקר לכדי טיפול קליני.[44]
שכיחות ואפידמיולוגיה
[עריכת קוד מקור | עריכה]המחלה פורצת לרוב אצל ילדים ומבוגרים צעירים.[45] רטיניטיס פיגמנטוזה היא הגורם המוביל לעיוורון על רקע תורשתי. תדירות המחלה נבדקה בעיקר בארצות הברית ובאירופה ועומדת על אחד מתוך 4,000 אנשים הלוקים בצורה הפשוטה (הלא סינדרומטית) של המחלה. בישראל היא גבוהה יותר, ובאזורים מסוימים עומדת על 1 מתוך 2,000 אנשים. ההערכה היא כי 1.5 מיליון אנשים ברחבי העולם מושפעים מהמחלה, נכון לשנת 2020.[46]
מחקר במרכז הרפואי הדסה ובאוניברסיטה העברית, הראה שהגורם העיקרי לראייה ירודה ולעיוורון בילדים במדינות מפותחות הוא מחלות רשתית על רקע תורשתי. המחקר נמשך קרוב לחמש שנים (2015–2019), ותוצאותיו הצביעו על מוטציות גנטיות כאחראיות למרבית לקויות הראייה ומחלות העיניים הגורמות לעיוורון, בהן רטיניטיס פיגמנטוזה.[47]
פרוגנוזה
[עריכת קוד מקור | עריכה]המחלה מוגדרת כפרוגרסיבית וחשוכת מרפא.[48]
בעוד עיוורון מוחלט הוא נדיר, חדות הראייה ושדה הראייה של האדם הלוקה במחלה ימשיכו לרדת ככל שמתמשכת התנוונות קולטני האור, בתחילה הקנים ולאחר מכן המדוכים. המחלה עלולה להוביל לעיוורון על-פי הגדרת החוק, ולעיוורון מלא בשלבי המחלה המתקדמים, אולם הראייה המרכזית יכולה להישאר יחסית טובה עד שלבים מאוחרים של המחלה.[49]
מחקר
[עריכת קוד מקור | עריכה]המחקר במחלות ניווניות של הרשתית החל בסוף המאה ה-19, עם התקדמות המכשור האופלטלמוסקופי, ומתקדם במקביל במספר תחומי מחקר.
השתלות רשתית
[עריכת קוד מקור | עריכה]המחקר מתמקד, בנוסף לפונקציונליות של ההשתלה, בבדיקת בטיחות של השתלת רקמת רשתית עצבית עוברית אנושית ואפיתל פיגמנט רשתית (RPE) לתוך עיניהם של חולים ברטיניטיס פיגמנטוזה. ההשתלה מבוצעת בעין עם הראייה הירודה יותר מבין שתי העיניים, וחייבת להיות בחדות ראייה מקסימלית של 20/200. השלמת אזורים פגועים ברשתית על ידי השתלת קולטני אור היא גישה מסורתית במחקר.[50]
שתלים מלאכותיים של רשתית
[עריכת קוד מקור | עריכה]בשנת 2012 החל ניסוי בהשתלת שבב ברשתית בניסיון לשקם את הראייה בחולי רטיניטיס פיגמנטוזה.[51][52]
מערכת שתל (דוגמת Argus II) הממוקמת על גבי הרשתית ומקובעת לעין בניתוח, בדומה לעדשה תוך עינית (אנ'), מצלמה זעירה ומערך צפוף של אלקטרודות מיקרוניות החודרות לרשתית ומעבירות אות חשמלי למרכז הראייה במוח דרך עצב הראייה. תוצאות מחקר קליני על יעילותו ובטיחותו של Argus II פורסמו ביוני 2015. המחקר, שכלל 30 משתתפים, מצא שיפור קל בתפקוד הראייה אצל מרבית הנבדקים.[53][54]
טיפול גנטי
[עריכת קוד מקור | עריכה]המחקר מתמקד בפיתוח טיפולים אופטוגנטיים, שמטרתם שחזור ראייה באופן מלא או חלקי. מחקר גנטי הוביל לטיפול חלקי בחולי רטיניטיס פיגמנטוזה ולפיתוח תרופה בשם לוקסטורנה שאושרה על ידי מינהל המזון והתרופות האמריקני (FDA) בשנת 2017.[55]
מחקר מתקדם (2024)
[עריכת קוד מקור | עריכה]- חברת Nanoscope Therapeutics האמריקנית נמצאת על סף הגשת בקשה (נכון למרץ 2024) לאישור ה-FDA של טיפול גנטי ראשון למחלה שניתן להשתמש בו ללא תלות במוטציות הגנטיות השונות.
המחקר מציג פיתוח מולקולה MCO-010 שלפי ניסויים קליניים הביא להישגים בעלי משמעות קלינית בחדות הראייה ובשדות ראייה. בנוסף, הדגים הניסוי פרופיל בטיחות חיובי.
הטיפול הוא אופטוגנטי אופייני (MCO) לשיקום הראייה ברטיניטיס פיגמנטוזה (RP) מתקדמת. חולים עם לקות ראייה חמורה עקב RP קיבלו זריקה תוך-זגוגיתית בודדת של MCO-010, בעוד שתשעה נוספים קיבלו זריקת דמה (פלצבו). התוצאות הראו שיפור בתפקוד הראייה לאחר טיפול ב-MCO-010 בהתאם למחקרים קודמים, וכן פרופיל בטיחות חיובי. התוצאות לאחר 12 חודשים הראו שאצל 16 מתוך 18 (88.9%) חולים שטופלו ב-MCO-010 היה שיפור משמעותי בחדות הראייה. בנוסף, הטיפול ב־MCO-010 נמצא נטול תופעות לוואי חמורות (עיניות או מערכתיות).[56]
במידה שהטיפול יאושר, הוא יהיה הטיפול הגנטי הראשון בהיסטוריה שיאפשר מענה לכלל חולי רטיניטיס פיגמנטוזה ברחבי העולם.[57]
באוקטובר 2024 פורסם כי טכניקת הטיפול הגנטי שיפרה משמעותית את הראייה בחולי רטיניטיס פיגמנטוזה רבים שאיבדו כמעט לחלוטין את ראייתם. התוצאות לאחר שנתיים של ניסוי קליני שלב 2b/3.[58]
- חברת Ocugen נמצאת בתחילת ניסוי (נכון לאפריל 2024) בטיפול גנטי (שלב III) OCU400 עבור רטיניטיס פיגמנטוזה. החברה הודיעה על עדכון מחקר חדש לתרופה (IND) שאושר על ידי מנהל המזון והתרופות האמריקאי (FDA). במחקר ישתתפו 150 חולים בשני סוגי ניסוי: חולים עם מוטציה בגן RHO וחולים בעלי גנים אגנוסטים. רופאי החברה מציינים כי הניסוי הקליני-אגנוסטי יספק אפשרות טיפולית מתאימה לכלל חולי רטיניטיס פיגמנטוזה.[59]
תאי גזע
[עריכת קוד מקור | עריכה]המחקרים הקשורים לתאי גזע הם מגוונים, ומשלבים מספר טכניקות שונות ליצירת תאי אור חדשים מתפקדים, אם מתוך תאים הקיימים ברשתית ואם בגידול תאים במעבדה והשתלתם ברשתית. מחקר שנעשה באקדמיה הצ'כית למדעים מתמקד בגידול תאי גזע פלוריפוטנטים (iPSCs), שהם תאי גזע שיכולים להתפתח לכל תא בגוף, כולל לתאי רשתית בריאים, שיאפשרו השתלתם והחלפה של מקטעי רשתית פגומים או של רשתית שלמה.[60][61]
תוספי תזונה
[עריכת קוד מקור | עריכה]לפי מחקר משנת 2023 של המכון לגנטיקה של העין (the Ocular Genomics Institute)[62] באוניברסיטת הרווארד, לוויטמין A אין כל יתרון עבור חולים במחלת העיניים רטיניטיס פיגמנטוזה.[63]
חומרים נוירוטרופים
[עריכת קוד מקור | עריכה]מחקר בחומרים נוירוטרופים (אנ'), שנערך בשנת 2012 על ידי מדענים מאוניברסיטת מיאמי, הציג נתונים המראים הגנה על קולטני האור של בעלי חיים שהוזרק לעיניהם גורם נוירוטרופי מזן אסטרוציטים (MANF).[64] חוקרים מאוניברסיטת קליפורניה בברקלי, הראו שתרופה שנועדה לגמילה מאלכוהוליזם מסייעת לשיפור תפקוד קולטני האור בעכברים עם ניוון ברשתית. התרופה מסייעת להפחית כמות של חומצה רטינואית המהווה מיסוך לראייה, ובכך עשויה לשחזר את הראייה בבני אדם הלוקים ברטיניטיס פיגמנטוזה.[65]
מחקר בתחום ביו-מולקולרי
[עריכת קוד מקור | עריכה]בשנת 2023 גילה צוות חוקרים מאוניברסיטת קליפורניה באירוויין נוגדן מיוחד שעשוי להוביל לטיפול ברטיניטיס פיגמנטוזה. החוקרים התמקדו במחקרם במולקולה ספציפית שלדעתם תספק טיפול לאופסין מסוג רודופסין, המהווה מולקולת חלבון מרכזית בחישת אור ברשתית האדם. המולקולה נמצאת בתאי קולטני האור, ומוטציות ברודופסין הן הגורם העיקרי ל-adRP (רטיניטיס פיגמנטוזה אוטוזומלית דומיננטית).[66]
זכויות סוציאליות ושיקום בקהילה
[עריכת קוד מקור | עריכה]במדינת ישראל חולי רטיניטיס פיגמנטוזה שמצבם מוגדר כעיוורון על פי חוק[67] או עיוורון מלא, זכאים לסיוע, לקצבאות ולשירותים שונים מגופים ממשלתיים דוגמת משרד הרווחה והביטחון החברתי, המוסד לביטוח לאומי ועמותות ייעודיות המתמחות במתן שירותים לעיוור, דוגמת המרכז לעיוור בישראל.[68] שירותים אלו כוללים אבחון במכונים לראייה ירודה, הדרכה שיקומית, ומתן עזרים שונים המסייעים ללקוי הראייה בהתמצאות במרחב, בקריאה ובארגון משק הבית.
תלמידים עיוורים ולקויי ראייה זכאים לסיוע ממשרד החינוך הכולל הנגשת סביבת הלמידה, סיוע בפרויקטים והכוונה חברתית.[69] המוסד לביטוח לאומי מסייע ללוקים בראייתם ללמוד במוסדות להשכלה גבוהה במסגרת שיקום מקצועי.[70]
המתקשים בהתמצאות במרחב הציבורי זכאים, לאחר מבחן התאמה, לקבל כלב נחייה שמסייע בהתניידות.[71][72]
רטיניטיס פיגמנטוזה במדיה האמנותית
[עריכת קוד מקור | עריכה]לאורך השנים נוצרו יצירות על ידי אנשים שלקו ברטיניטיס פיגמנטוזה, המתארות את חוויית החיים עם המחלה, את האתגר, הקשיים הקשורים להתמודדות במסגרת האישית המשפחתית והקהילתית, ואת תהליכי השיקום והצמיחה האישית.
- הספר "רטיניטיס פיגמנטוזה" שכתב אהרון ירושלמי (ישראל, 2007), מספר על התמודדות של זוג העובר לבית מוגן, ומתאר את התסכולים והקשיים הקשורים בהתמודדות עם המחלה.[73]
- הסרט "Borealis" (קנדה, 2015), מספר את סיפורה של אורורה בת ה-15 והתמודדותה עם המחלה ברקע קשיים משפחתיים. בסרט כמה סצנות מנקודת מבטם של הלוקים ברטיניטיס פיגמנטוזה ומתארים ראיית מנהרה.[74]
- ההצגה "בלי עין הרע" (ישראל, 2021), היא סיפורו של השחקן אסף בן שמעון, ומתארת את אובדן הראייה שלו ואת מסעו להגשמת חלום הבמה והתיאטרון.[75]
- בסרט "מבוא לאושר" (ארצות הברית, 2023), אחד מגיבורי המשנה חולה במחלה ומשתף את חוויית תהליך איבוד הראייה, את הקושי לראות בחושך, ואת פרישתו בשל המחלה מעיסוקו כרופא מטפל.[76]
- הסרט "Blink"(אנ') (ארצות הברית, 2024), הוא סרט תיעודי אמריקאי בבימויו של אדמונד סטנסון ודניאל רוהר, העוקב אחר משפחה קנדית שמטיילת מסביב לעולם לפני שילדיה מאבדים את ראייתם כתוצאה מרטיניטיס פיגמנטוזה, כדי לחוות את יופיו של העולם בזמן שהם עדיין יכולים.[77]
קהילת לראות רחוק
[עריכת קוד מקור | עריכה]קהילת "לראות רחוק" היא קהילת החולים ברטיניטיס פיגמנטוזה במדינת ישראל ומהווה משענת לחולים ולבני משפחותיהם. את הקהילה ייסד בשנת 2019 יוסי סעידוב, פעיל ויזם חברתי הלוקה בעצמו במחלה. הקהילה מתפקדת בשיתוף פעולה עם עמותת "לראות", שנטלה על עצמה את האתגר להגביר את המודעות החברתית והמאמץ המחקרי בתחום בריאות העין, במטרה לאתר טיפולים למיגור מחלות הגורמות לעיוורון, ובכללן רטיניטיס פיגמנטוזה.[78]
במסגרת פעילות הקהילה מתקיימים כנסים, הצגות תיאטרון ותערוכות בתחום בריאות העין וההתמודדות הייחודית של החולים ברטיניטיס פיגמנטוזה.[79][80] ביולי 2023 התקיימה בתל אביב התערוכה "נקודת מבט", המאפשרת למבקרים בה לחוות ראיית מנהרה: עיוורון חלקי המאפיין את הלוקים במחלה.[81]
ראו גם
[עריכת קוד מקור | עריכה]לקריאה נוספת
[עריכת קוד מקור | עריכה]- Peter M.J. Quinn, Retinitis Pigmentosa, Department of Ophthalmology, Columbia University, 2023
קישורים חיצוניים
[עריכת קוד מקור | עריכה] אתר האינטרנט הרשמי של משפחת לראות רחוק - קהילת רטיניטיס פיגמנטוזה בישראל
אתר האינטרנט הרשמי של משפחת לראות רחוק - קהילת רטיניטיס פיגמנטוזה בישראל- Jason Hsu., Retinitis Pigmentosa, American Academy of Ophthalmology-Eyewiki, March 10, 2024
- רטיניטיס פיגמנטוזה באתר העמותה למחקר בריאות העין ומניעת העיוורון בישראל
- רטיניטיס פיגמנטוזה, באתר אנציקלופדיה בריטניקה (באנגלית)
 Retinitis Pigmentosa, סרטון בערוץ "Craig Blackwell", באתר יוטיוב (אורך: 40:05)
Retinitis Pigmentosa, סרטון בערוץ "Craig Blackwell", באתר יוטיוב (אורך: 40:05)
הערות שוליים
[עריכת קוד מקור | עריכה]- ^ 1 2 3 Hereditary retinal disease (עמ' 17-18), באתר oftalmic
- ^ Fraser Muirhead, Adrien van Trigt, and the first published ophthalmoscopic images (De Speculo Oculi, 1853), Journal of Medical Biography 29, 2021-11, עמ' 221–228 doi: 10.1177/0967772020914795
- ^ Sanne K. Verbakel, Ramon A. C. van Huet, Camiel J. F. Boon, Anneke I. den Hollander, Rob W. J. Collin, Caroline C. W. Klaver, Carel B. Hoyng, Ronald Roepman, B. Jeroen Klevering, Non-syndromic retinitis pigmentosa, Progress in Retinal and Eye Research 66, 2018-09-01, עמ' 157–186 doi: 10.1016/j.preteyeres.2018.03.005
- ^ Helga Kolb, Simple Anatomy of the Retina , med
- ^ Navid Mahabadi, Yasir Al Khalili, Neuroanatomy, Retina, Treasure Island (FL): StatPearls Publishing, 2024
- ^ Human eye | Definition, Anatomy, Diagram, Function, & Facts, Encyclopedia Britannica, 16 בספטמבר 1998
- ^ Kevin H. Nguyen, Bhupendra C. Patel, Prasanna Tadi, Anatomy, Head and Neck: Eye Retina, Treasure Island (FL): StatPearls Publishing, 2025
- ^ S Natarajan, Retinitis pigmentosa, NCBI
- ^ עילית בור, הדס קליש, חידושים באבחנות ובטיפולים לרטיניטיס פיגמנטוזה עמ׳ 33, באתר Medicine כתב עת רפואי בנושא רפואת עיניים, מרץ - אפריל 2010
- ^ Sabnis, Mohta, Nayyar, Kulkarni, Retinitis Pigmentosa in a rare case of Bardet Beidl Syndrome 4, 2019, עמ' 499
- ^ Marilita Moschos, Alexandras Chatzirallis, and Irini Chatziralli, Psychological Aspects and Depression in Patients with Retinitis Pigmentosa, באתר sagepub, 3 במאי 2015
- ^ Sandra Cottet, Daniel F. Schorderet, Mechanisms of apoptosis in retinitis pigmentosa, Current Molecular Medicine 9, 2009-04, עמ' 375–383 doi: 10.2174/156652409787847155
- ^ Fay Newton, Mechanisms of Photoreceptor Death in Retinitis Pigmentosa, ncbi
- ^ Dikla Bandah-Rozenfeld, Liliana Mizrahi-Meissonnier, Chen Farhy, Alexey Obolensky, Homozygosity Mapping Reveals Null Mutations in FAM161A as a Cause of Autosomal-Recessive Retinitis Pigmentosa, American Journal of Human Genetics 87, 2010-09-10, עמ' 382–391 doi: 10.1016/j.ajhg.2010.07.022
- ^ Retinitis pigmentosa and allied diseases: numerous diseases, genes, and inheritance patterns, באתר Human Molecular Genetics, 15 במאי 2002
- ^ מחלות אלה הן תורשתיות וקשורות לגן הממוקם על כרומוזום X
- ^ Clinics, Epidemiology and Genetics of Retinitis Pigmentosa, באתר ncbi
- ^ SP Daiger, LS Sullivan, SJ Bowne, Genes and mutations causing retinitis pigmentosa, באתר ncbi
- ^ Uwe Wolfrum, Eyal Banin, Dror Sharon, A new mouse model for retinal degeneration due to Fam161a deficiency, Scientific Reports 11, 2021-01-21, עמ' 2030 doi: 10.1038/s41598-021-81414-1
- ^ John Gray, Nallur Basappa Ramachandra, Tomer Avidor-Reiss, The evolution of centriole degradation in mouse sperm, Nature Communications 15, 2024-01-02, עמ' 117 doi: 10.1038/s41467-023-44411-8
- ^ Tamar Ben-Yosef, Dror Sharon, Eyal Banin, Unique combination of clinical features in a large cohort of 100 patients with retinitis pigmentosa caused by FAM161A mutations, Scientific Reports 10, 2020-09-16, עמ' 15156 doi: 10.1038/s41598-020-72028-0
- ^ רטיניטיס פיגמנטוזה (Retinitis pigmentosa) - הסימפטומים, הבדיקות ודרכי הטיפול, באתר Infomed
- ^ Comprehensive Adult Medical Eye Evaluation, American Academy of Ophthalmology
- ^ אלקטרורטינוגרפיה (electroretinography), באתר Infomed
- ^ רטיניטיס פיגמנטוזה (RP): לראות את העולם דרך צינור, באתר www.clalit.co.il
- ^ Doctors - רטיניטיס פיגמנטוזה: יש אור?, באתר Doctors
- ^ צילום קרקעית העין לאחר הזרקת פלואורסצאין (fluorescein angiography) - על הבדיקה, הסיכונים והתהליך, באתר Infomed
- ^ J. T. Pearlman, T. P. Flood, S. R. Seiff, Retinitis pigmentosa without pigment, American Journal of Ophthalmology 81, 1976-04, עמ' 417–419 doi: 10.1016/0002-9394(76)90296-8
- ^ רטיניטיס פיגמנטוזה (RP - Retinitis Pigmentosa), באתר מגדלור - מכון לראיה ירודה, 13 באוגוסט 2020
- ^ Razek Georges Coussa, Diana Basali, Akiko Maeda, Meghan DeBenedictis, and Elias I. Traboulsicorresponding author, Sector retinitis pigmentosa: Report of ten cases and a review of the literature, באתר ncbi
- ^ J. V. Bastek, R. Y. Foos, J. Heckenlively, Traumatic pigmentary retinopathy, American Journal of Ophthalmology 92, 1981-11, עמ' 621–624 doi: 10.1016/s0002-9394(14)74652-5
- ^ Causes of Pseudo-Retinitis Pigmentosa, Eyedocs (באנגלית)
- ^ Sanne K. Verbakel, Ramon A. C. van Huet, Camiel J. F. Boon, Anneke I. den Hollander, Rob W. J. Collin, Caroline C. W. Klaver, Carel B. Hoyng, Ronald Roepman, B. Jeroen Klevering, Non-syndromic retinitis pigmentosa, Progress in Retinal and Eye Research 66, 2018-09-01, עמ' 157–186 doi: 10.1016/j.preteyeres.2018.03.005
- ^ Usher syndrome, Retina UK
- ^ Stephen H. Tsang, Peter M. J. Quinn, Retinitis Pigmentosa, Springer Nature, 2022-12-08, עמ' 25, ISBN 978-1-0716-2651-1
- ^ G. de la Mata Pérez, O. Ruiz-Moreno, S. Fernández-Pérez, C. Torrón Fernández-Blanco, L. Pablo-Júlvez, Retinitis pigmentosa sine pigmenti. Debut with macular oedemaRetinosis pigmentaria sine pigmento. Inicio con edema macular☆
- ^ Kearns Sayre Syndrome - Symptoms, Causes, Treatment | NORD, rarediseases.org
- ^ Chronic granulomatous disease, the McLeod phenotype and the contiguous gene deletion syndrome-a review, ncbi
- ^ Refsum disease: MedlinePlus Genetics, medlineplus.gov
- ^ Bardet-Biedl syndrome (BBS), Retina UK
- ^ ד"ר יונת אשחר, אושר טיפול גֵני ראשון למחלת עיניים ניוונית, במדור "חדשות מדע" באתר של מכון דוידסון לחינוך מדעי, 25 בדצמבר 2017
- ^ Office of the Commissioner, FDA approves novel gene therapy to treat patients with a rare form of inherited vision loss, FDA, 2020-03-24 (באנגלית)
- ^ How does LUXTURNA work?, luxturna
- ^ Nanoscope Therapeutics Announces Positive Top-line Results from Randomized Controlled Trial of MCO-010 for Retinitis Pigmentosa - Nanoscope Therapeutics, 2024-03-26
- ^ ורוניקה צור הלפרין, רטיניטיס פיגמנטוזה, באתר www.hac.ac.il
- ^ איל בנין ואיתי חוברס, גישות נסיוניות לטיפול ברטיניטיס פיגמנטוזה, הרפואה, כרך 143, מאי 2004, עמ' 91
- ^ האוניברסיטה העברית, בניגוד לעבר: מחלות תורשתיות הן הגורם העיקרי לראיה ירודה ועיוורון בילדים בישראל, באתר "הידען", 3 בנובמבר 2021
- ^ למעט טיפול גנטי אצל ילדים הלוקים במוטציות בגן RPE65, אין למחלה טיפול יעיל.
- ^ רטיניטיס פיגמנטוזה (RP) - לראות את העולם דרך צינור, באתר redirect.clalit.co.il
- ^ Safety Study in Retinal Transplantation for Retinitis Pigmentosa, באתר clinicaltrials
- ^ ד"ר איתי גל, שבב אלקטרוני הושתל בשני עיוורים - שחזרו לראות, באתר ynet, 3 במאי 2012
- ^ אריאלה איילון, בילינסון: שבב אלקטרוני הושתל בעיניה של עיוורת - שתחזור לראות, באתר ynet, 6 במאי 2021
- ^ Mohsen Farvardin, The Argus-II Retinal Prosthesis Implantation, Frontiers in Neuroscience 12, 2018 doi: 10.3389/fnins.2018.00584/full
- ^ שתל רשתית מלאכותית, מחלות ניווניות תורשתיות של הרשתית | Bewell| איכילוב
- ^ Phil Taylor, Nanoscope Therapeutics to Present at the Next Generation Ophthalmic Drug Delivery Summit, 26 March, 2024
- ^ David S Boyer; Lance Bergstrom; Andres Emanuelli; Victor H Gonzalez; Charles Clifton Wykoff; Sunil Gupta; David S Liao; Vitaliy Zak; Sai H Chavala; Samar Mohanty; subrata bataybal; Jody Piltz-Seymour; Ananta Ayyagari; John Koester; Aaron Osborne, Efficacy and safety of MCO-010 optogenetic therapy for vision restoration in patients with severe vision loss due to retinitis pigmentosa: A phase 2b randomized, sham-controlled, multi-center, multi-dose, double-masked clinical trial (RESTORE), iovs.arvojournals.org, June 2023
- ^ Nanoscope preps filing for retinitis pigmentosa gene therapy, pharmaphorum, 2024-03-26 (באנגלית)
- ^ Don Sapatkin, A New Type of Gene Therapy Shows Promise for Treating Retinitis Pigmentosa, Managed Healthcare Executive, 21 באוקטובר 2024
- ^ Abigail Beaney, Ocugen to initiate Phase III trial of gene therapy for retinitis pigmentosa, Clinical Trials Arena, 10 באפריל 2024
- ^ Ana Artero Castro, Dunja Lukovic, Pavla Jendelova, Slaven Erceg, Concise Review: Human Induced Pluripotent Stem Cell Models of Retinitis Pigmentosa, Stem Cells (Dayton, Ohio) 36, 2018-04, עמ' 474–481 doi: 10.1002/stem.2783
- ^ חשיפה: בנק "איברים זעירים" הראשון מסוגו בארץ הוקם במרכז הרפואי הדסה, באתר ynet, 24 ביוני 2022
- ^ Ocular Genomics Institute, eye.hms.harvard.edu
- ^ Eric Pierce, New Report: Vitamin A Supplementation Provides No Vision Benefit to RP Patients, Foundation Fighting Blindness, 2 בנובמבר 2023
- ^ Rong Wen, Lingyu Luo, Dequang Huang, Xin Xia, Zhengying Wang, Pingping Chen, Yiwen Li, Mesencephalic Astrocyte-derived Neurotrophic Factor (MANF) Protects Rod and Cone Photoreceptors from Degeneration in Transgenic Rats Carrying the S334ter Rhodopsin Mutation, Investigative Ophthalmology & Visual Science
- ^ Robert S, ers, Media relations|, Antabuse may help revive vision in people with progressive blinding disorders, Berkeley News, 18 במרץ 2022
- ^ UC Irvine researchers discover a nanobody which may lead to treatment for Retinitis Pigmentosa | UCI School of Medicine, medschool.uci.edu
- ^ הגדרת עיוור, באתר כל זכות
- ^ המרכז לעיוור בישראל
- ^ הנגשות לתלמידי בית ספר עיוורים ולקויי ראייה, באתר כל זכות
- ^ שיקום מקצועי - קצבאות והטבות | ביטוח לאומי, באתר www.btl.gov.il
- ^ מרכז ישראלי לכלבי נחייה, באתר IGD - Israel Dog Guide
- ^ קצבה לאחזקת כלב נחייה, באתר כל זכות
- ^ אהרון ירושלמי, רטיניטיס פיגמנטוזה, הוצאת טרקלין, 2007
- ^ Borealis, באתר imdb
- ^ אסף בן שמעון, שראל פיטרמן, בלי עין הרע, באתר תאטרון נפש
- ^ Happiness For Beginners Ending Explained - What Pablo Neruda's Poem Really Means, IMDb
- ^ Blink, 2024 באתר IMDb
- ^ עמותת לראות, באתר www.eyes.org.il
- ^
 תיאטרון פלייבק למתמודדים עם מחלות רשתית גנטיות - קהילת לראות רחוק, סרטון בערוץ "Yossi Saidov", באתר יוטיוב (אורך: 01:41)
תיאטרון פלייבק למתמודדים עם מחלות רשתית גנטיות - קהילת לראות רחוק, סרטון בערוץ "Yossi Saidov", באתר יוטיוב (אורך: 01:41)
- ^ רטיניטיס פיגמנטוזה-RP - קהילת לראות רחוק | Facebook, באתר www.facebook.com
- ^ מירי בן-דוד ליוי, "ראיית צינור": לחוש בתערוכה איך רואים חולי רטיניטיס פיגמנטוזה, באתר ynet, 17 ביולי 2023
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.





